产品优势
1.与二代单细胞转录组测序相比,利用长读长优势,获得单细胞水平上的全长转录本数据,实现真正意义上的全长读取,特别是在实验样本获得困难,例如特殊处理的细胞或发育早期刚分化的基元细胞,细胞数目偏少的情况下,通过纳米孔单细胞全长转录组测序,可获得全长转录本进行转录组数据分析。获得的全长转录本,能够发现许多短读长测序遗漏的新转录本;且能够准确进行可变剪切位点分析,同时将这些剪接事件关联至对应的转录本,发现更多的isoform。此项特有优势为研究单细胞水平上的可变剪接、基因融合事件、基因结构分析、基因注释及筛选等提供有力保障。
2.与纳米孔三代全长转录组测序相比,解决因细胞异质性而导致重要基因表达量无法准确检测的问题。在某些样本中,例如组织样本、血液样本,由于样本内的细胞组成并不是单一化的,或者因为某类占主导的细胞群体基因表达较高,而掩盖了少量细胞群体的基因表达情况。常规的RNA混池测序(Bulk测序)无法准确判断某类细胞群体的基因表达量,而单细胞测序可以很好的解决这一类问题。
3.与10x单细胞标记联合PacBio进行单细胞全长转录组测序相比,纳米孔单细胞全长转录组测序成本较低,一张PromethION芯片所获得reads可达50M(内部测序数据),远多于PacBio产生的reads数。
方案策略
请提前联系当地科技顾问。
分析内容
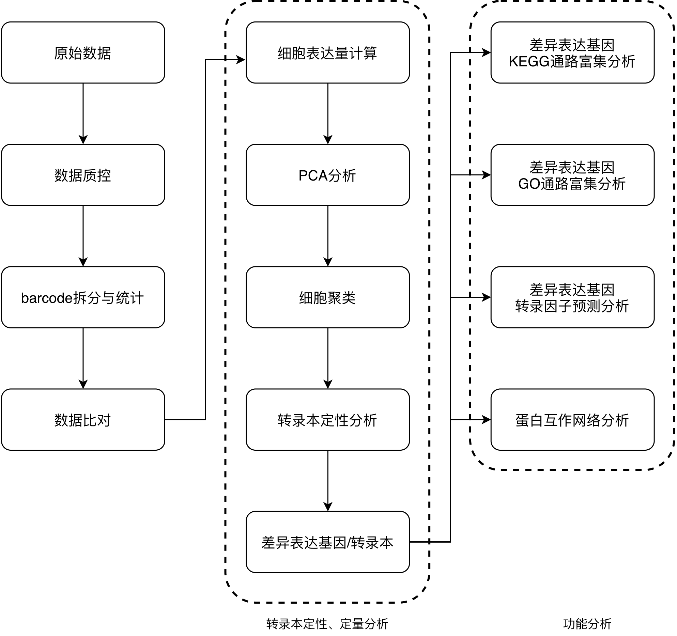
结果展示
单细胞转录本结构分析
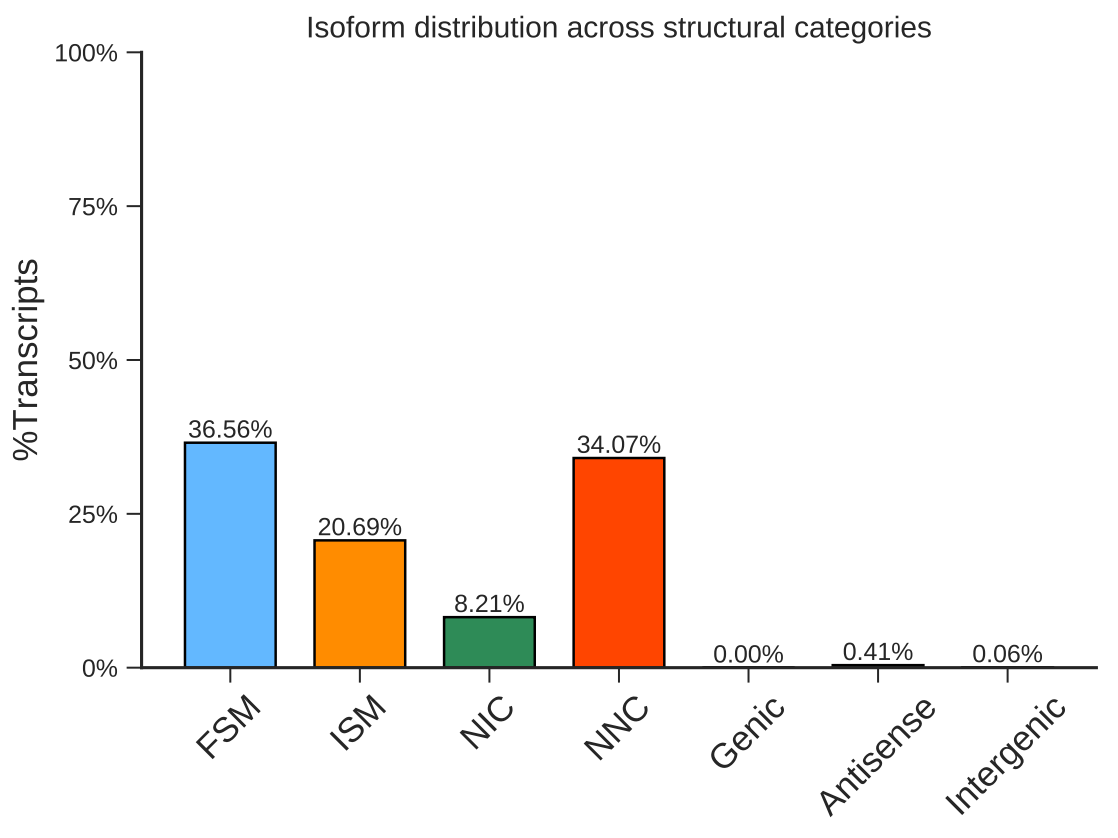
单细胞转录本可变剪接检测
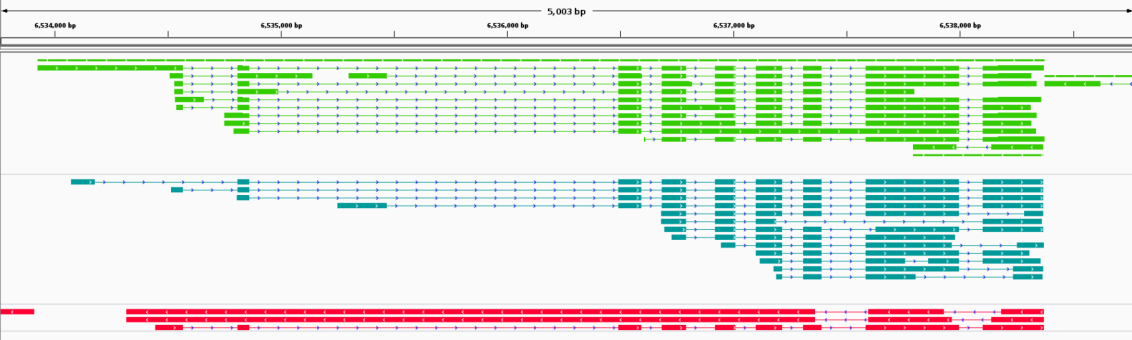
细胞聚类和特征基因筛选
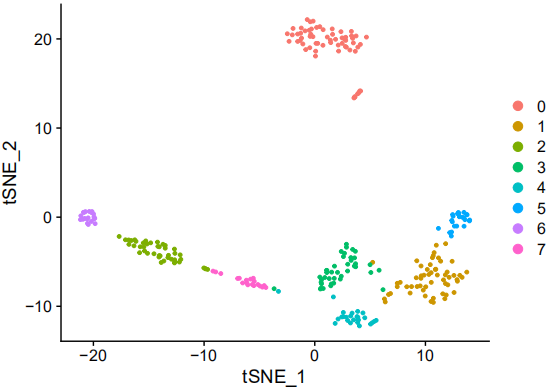
常见问题
1.纳米孔单细胞全长转录组和smart-seq2全长转录组之间的区别是什么?
答:主要是测序平台上的差异。纳米孔单细胞全长转录组是利用Nanopore平台,可以实现全长转录组的测序,而smart-seq2全长转录组是利用二代测序平台,无法实现真正意义上的全长转录组测序。
2.细胞起始量只有1-500个,能不能多点?
答:我们会采纳建议,开发针对样本量大的纳米孔单细胞全长转录组测序。
案例解析
案例分析一
案例解析
10x单细胞转录组结合纳米孔全长转录组测序
将Nanopore测序技术与UMI以及10xGenomics单细胞分离系统相结合的方法,以获得经过纠错的全长序列信息。这一方法使在单细胞水平上检测差异RNA剪接和RNA编辑成为可能。
本研究设计了可以高效可靠的将cellBC和UMI分配到Nanopore reads的策略。首先利用Illumina对10xGenomics文库进行短读测序,为每个基因和基因组区域定义相关的cellBC,然后为每个细胞、基因或基因组区域定义相关的UMIs组合。随后利用上述信息指导cellBC和UMI分配到已经比对至基因组的Nanopore reads上。
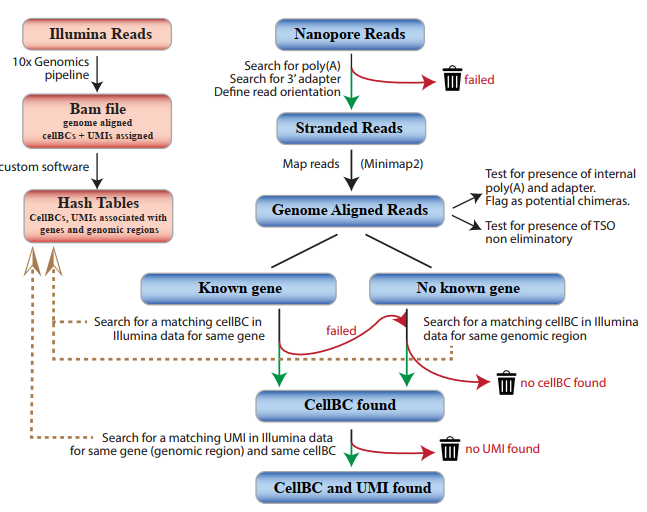 图1 CellBC 与 UMI 分配策略
图1 CellBC 与 UMI 分配策略
研究者使用10×Genomics制备了190和951个E18小鼠大脑细胞文库,随后分别用Illumina和Nanopore测序。UMls分子条码能够使嵌合cDNA被错误地注释为新转录本的风险降至最低。但是,先前的研究未能在单细胞纳米孔测序中使用UMls。本研究的UMl分配策略中,将97.4%的UMI分配给76%的已鉴定cellBC的Nanopore reads(图2b,c)。通过二代测序测序在单细胞中鉴定到的UMIs和基因分,别有75%和82%同样在Nanopore数据集中找到,并且Nanopore与二代测序之间的基因表达相关性也很好(图2e-g)。因此,该策略cellBC和UM1指定的Nanopore数据集很好地代表了10xGenomics方法中捕获的转录组。
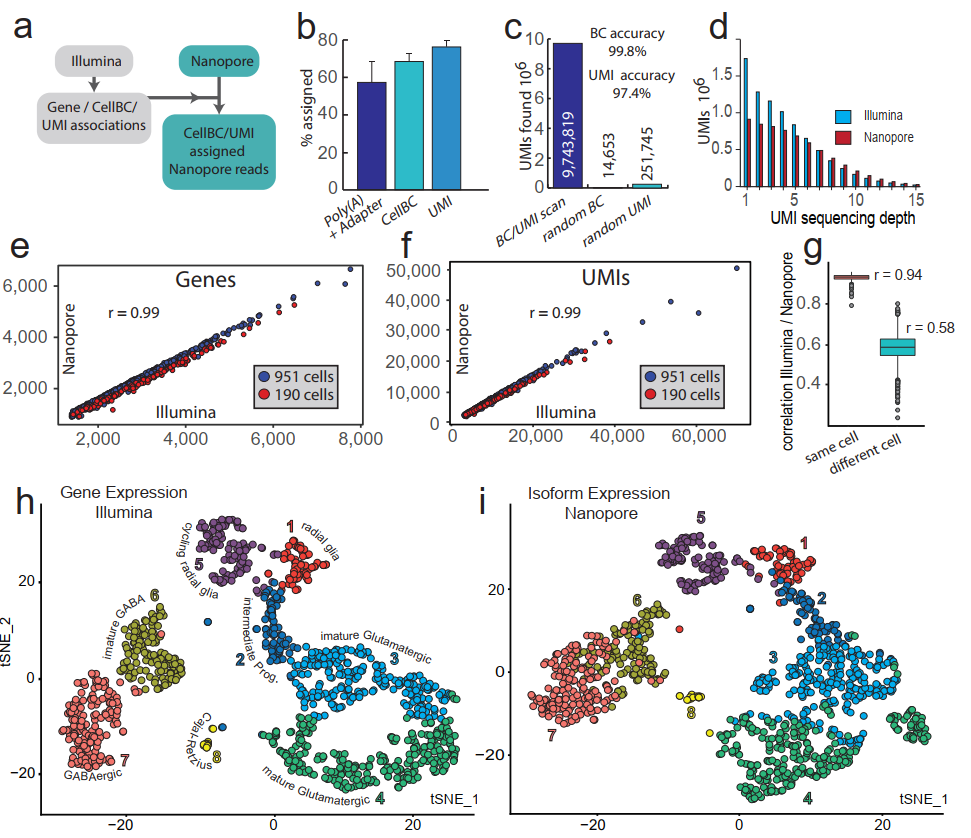 图2 Nanopore单细胞转录组测序。(a)Cell barcode与UMI 分配策略;(b,c)Cell barcode与UMI 分配效率(b)与准确度(c);(d)Illumina和Nanopore数据集的UMI测序深度; (e,f)通过Illumina和Nanopore测序,检测1141个细胞的基因数量(e)和UMIs数量(f);(g)Illumina和Nanopore测序数据之间的基因表达相关性;(h,i)Illumina基因表达(h)和Nanopore转录异构体表达(i)的t-SNE图。
图2 Nanopore单细胞转录组测序。(a)Cell barcode与UMI 分配策略;(b,c)Cell barcode与UMI 分配效率(b)与准确度(c);(d)Illumina和Nanopore数据集的UMI测序深度; (e,f)通过Illumina和Nanopore测序,检测1141个细胞的基因数量(e)和UMIs数量(f);(g)Illumina和Nanopore测序数据之间的基因表达相关性;(h,i)Illumina基因表达(h)和Nanopore转录异构体表达(i)的t-SNE图。
Nanopore与二代测序确定的E18小鼠大脑典型的细胞类型t-SNE图显示出相似的聚类(图1 h,i)。研究者进一步寻找到139个在簇间具有差异转录异构体表达的基因,例如网格蛋白轻链A (Clta)在神经元成熟过程中经历明显的异构体转换(图3 a-d),异构体转换可能对该蛋白在不同发育阶段的作用进行微调。
研究者通过对相同UMI的reads进行分组,来纠正Nanopore测序错误,为每个RNA分子生成一致序列,并在单个细胞内识别这种序列异质性(图3 e,f)。通过对Gria2校正后的一致性序列分析,证实了之前关于Gria2编辑的发现,并且揭示了一个位点的编辑增加了另一个位点被编辑的可能性(图3 g)。因此,单细胞长读测序既证实又扩展了之前关于中枢神经系统中Gria2编辑的知识。
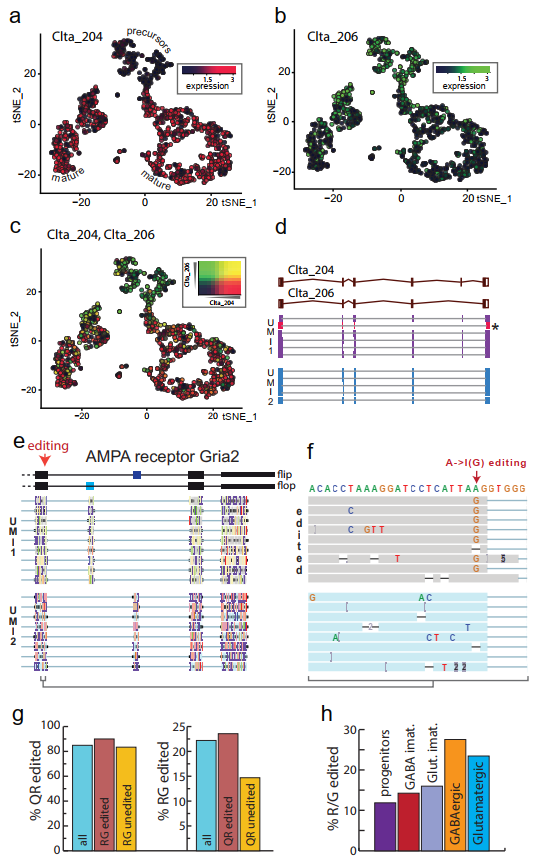 图3 Nanopore单细胞转录组测序显示转录本多样性。(a-c)t-SNE图显示了神经元成熟过程中的Clta亚型表达开关;(d)两个UMIs的主要Clta剪接变异体和支持的基因组比对read;(e)Gria2的主要剪接变体;(f)R/G A->I 编辑位点放大;(g)Q/R和R/G编辑;(h)在神经元成熟期间,R / G位点的A-> I编辑扩展会增加。
图3 Nanopore单细胞转录组测序显示转录本多样性。(a-c)t-SNE图显示了神经元成熟过程中的Clta亚型表达开关;(d)两个UMIs的主要Clta剪接变异体和支持的基因组比对read;(e)Gria2的主要剪接变体;(f)R/G A->I 编辑位点放大;(g)Q/R和R/G编辑;(h)在神经元成熟期间,R / G位点的A-> I编辑扩展会增加。
参考文献:
Lebrigand K, Magnone V, Barbry P, et al. High throughput, error corrected Nanopore single cell transcriptome sequencing[J]. bioRxiv, 2019: 831495.



